前回の続き・・・。
7 月 8 日(金)に開催された第 81 回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和 4 年度第 5 回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)における“血小板減少症を伴う血栓症( TTS )”を報告する。
≪血小板減少症を伴う血栓症( TTS )≫
【ファイザー社製】
1. 報告状況
○ 前回の集計対象期間( 5 月 15 日)以降、コミナティ筋注の副反応疑い報告において、製造販売業者から血栓症(血栓塞栓症を含む。)(血小板減少症を伴うものに限る。)( TTS )疑いとして報告されたて報告された事例に増加は無く(うち、 4 回目接種後の事例の増加は 0 件)あり、令和 3 年 8 月 3 日から令和 4 年 6 月 12 日までに報告された TTS 疑い事例は計 54 件(うち、 4 回目接種後の事例は 0 件)となった。
2. 専門家の評価
○ 令和 4 年 6 月 12 日までに報告された 54 事例を対象に、専門家の評価を実施。
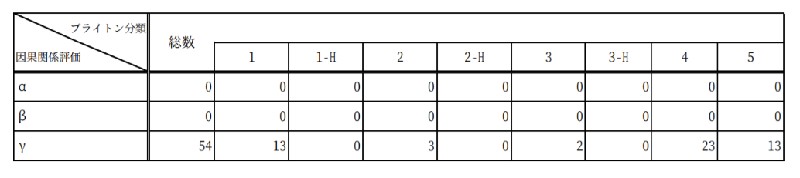
○ 「ブライトン分類」での評価は、 54 事例中、重篤とされている“ 3 ”以上に該当するのは 18 例となっている。
・ レベル 1 ~ 3 の報告件数/推定接種回数・・・ 18 件/ 125,210,770 回接種
・ 100 万回あたりの報告件数・・・ 0.1 件
○ブライトン分類レベル 1 ~ 3 の年齢別・性別の報告件数
| 年齢(歳) | 報告件数 | |||
|---|---|---|---|---|
| 男性 | 女性 | 性別不明 | ||
| 0~4 | 0 | 0 | 0 | 0 |
| 5~9 | 0 | 0 | 0 | 0 |
| 10~14 | 0 | 0 | 0 | 0 |
| 15~19 | 0 | 0 | 0 | 0 |
| 20~24 | 0 | 0 | 0 | 0 |
| 25~29 | 0 | 0 | 0 | 0 |
| 30~34 | 0 | 0 | 0 | 0 |
| 35~39 | 1 | 0 | 1 | 0 |
| 40~44 | 1 | 1 | 0 | 0 |
| 45~49 | 1 | 1 | 0 | 0 |
| 50~54 | 0 | 0 | 0 | 0 |
| 55~59 | 3 | 3 | 0 | 0 |
| 60~64 | 1 | 1 | 0 | 0 |
| 65~69 | 1 | 0 | 1 | 0 |
| 70~74 | 4(-1) | 2(-1) | 2 | 0 |
| 75~79 | 1 | 1 | 0 | 0 |
| 80歳以上 | 4 | 1 | 3 | 0 |
| 不明 | 1 | 1 | 0 | 0 |
| 合計 | 18 | 11 | 7 | 0 |
| (参考) 65歳以上 |
10 | 4 | 6 | 0 |
| (参考) 12~17 |
0 | 0 | 0 | 0 |
| (参考) 18~24 |
0 | 0 | 0 | 0 |
〔考察〕 前回から、変更なし。
【モデルナ社製】
1. 報告状況
○ 前回の集計対象期間( 5 月 15 日)以降、スパイクバックス筋注の副反応疑い報告において、製造販売業者から血栓症(血栓塞栓症を含む。)(血小板減少症を伴うものに限る。)( TTS )疑いとして報告された事例が 1 件増加し(うち、 4 回目接種後の事例は 0 件)、令和 3 年 8 月 3 日から令和 4 年 6 月 12 日までに報告された TTS 疑い事例は計 12 件(うち、 4 回目接種後の事例は 0 件)となった。
2. 専門家の評価
○ 令和 4 年 5 月 15 日までに報告された 12 事例を対象に、専門家の評価を実施。
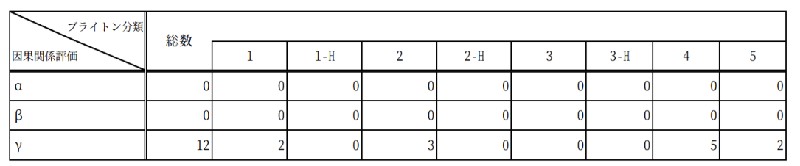
○ 「ブライトン分類」での評価は、 12 事例中、重篤とされている“ 3 ”以上に該当するのは 5 例となっている。
・ レベル 1 ~ 3 の報告件数/推定接種回数・・・ 5 件/ 52,727,969 回接種
・ 100 万回あたりの報告件数・・・ 0.1 件
○ブライトン分類レベル 1 ~ 3 の年齢別・性別の報告件数
| 年齢(歳) | 報告件数 | |||
|---|---|---|---|---|
| 男性 | 女性 | 性別不明 | ||
| 0~4 | 0 | 0 | 0 | 0 |
| 5~9 | 0 | 0 | 0 | 0 |
| 10~14 | 0 | 0 | 0 | 0 |
| 15~19 | 1 | 0 | 1 | 0 |
| 20~24 | 0 | 0 | 0 | 0 |
| 25~29 | 0 | 0 | 0 | 0 |
| 30~34 | 0 | 0 | 0 | 0 |
| 35~39 | 1(+1) | 0 | 1(+1) | 0 |
| 40~44 | 0 | 0 | 0 | 0 |
| 45~49 | 1 | 1 | 0 | 0 |
| 50~54 | 1 | 1 | 0 | 0 |
| 55~59 | 1 | 1 | 0 | 0 |
| 60~64 | 0 | 0 | 0 | 0 |
| 65~69 | 0 | 0 | 1 | 0 |
| 70~74 | 0 | 0 | 0 | 0 |
| 75~79 | 0 | 0 | 0 | 0 |
| 80歳以上 | 0 | 0 | 0 | 0 |
| 不明 | 0 | 0 | 0 | 0 |
| 合計 | 5(+1) | 3 | 2(+1) | 0 |
| (参考) 65歳以上 |
0 | 0 | 0 | 0 |
| (参考) 12~17 |
1 | 0 | 1 | 0 |
| (参考) 18~24 |
0 | 0 | 0 | 0 |
〔考察〕 モデルナ社に関しては中年層に偏っている傾向が続きそうだ。
【アストラゼネカ社製】
1. 報告状況
○ 前回の集計対象期間( 5 月 15 日)以降、バキスゼブリア筋注の副反応疑い報告において、製造販売業者から血栓症(血栓塞栓症を含む。)(血小板減少症を伴うものに限る。)( TTS )疑いとして報告された事例に増加はなく、令和 3 年 8 月 3 日から令和 4 年 6 月 12 日までに報告された TTS 疑い事例は計 2 件(うち、 4 回目接種後の事例は 0 件)となった。
2. 専門家の評価
○ 令和 4 年 6 月 12 日までに報告された 2 事例を対象に、専門家の評価を実施。
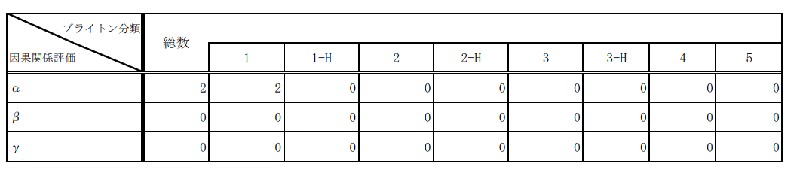
○「ブライトン分類」での評価は、 2 事例中、重篤とされている“ 3 ”以上に該当するのは 2 例となっている。
・ レベル 1 ~ 3 の報告件数/推定接種回数・・・ 2 件/ 117,366 回接種
・ 100 万回あたりの報告件数・・・ 17.0 件
○ブライトン分類レベル 1 ~ 3 の年齢別・性別の報告件数
| 年齢(歳) | 報告件数 | |||
|---|---|---|---|---|
| 男性 | 女性 | 性別不明 | ||
| 0~4 | 0 | 0 | 0 | 0 |
| 5~9 | 0 | 0 | 0 | 0 |
| 10~14 | 0 | 0 | 0 | 0 |
| 15~19 | 0 | 0 | 0 | 0 |
| 20~24 | 0 | 0 | 0 | 0 |
| 25~29 | 0 | 0 | 0 | 0 |
| 30~34 | 0 | 0 | 0 | 0 |
| 35~39 | 0 | 0 | 0 | 0 |
| 40~44 | 0 | 0 | 0 | 0 |
| 45~49 | 1 | 1 | 0 | 0 |
| 50~54 | 0 | 0 | 0 | 0 |
| 55~59 | 0 | 0 | 0 | 0 |
| 60~64 | 0 | 0 | 0 | 0 |
| 65~69 | 0 | 0 | 0 | 0 |
| 70~74 | 1 | 1 | 0 | 0 |
| 75~79 | 0 | 0 | 0 | 0 |
| 80歳以上 | 0 | 0 | 0 | 0 |
| 不明 | 0 | 0 | 0 | 0 |
| 合計 | 2 | 2 | 0 | 0 |
| (参考) 65歳以上 |
1 | 1 | 0 | 0 |
| (参考) 12~17 |
0 | 0 | 0 | 0 |
| (参考) 18~24 |
0 | 0 | 0 | 0 |
〔考察〕 接種数が少ない為、統計としてみるのは難しいようだ。また、現時点では、男性のみに発生している。
〔総考察〕 今回も血小板減少症を伴う血栓症( TTS )に関する論点のまとめ等は記載されていない。ファイザー社、モデルナ社、アストラゼネカ社も、データとしてはこれと言って取り上げるほどのものではなかった。
次回へ・・・。













