前回の続き・・・。
前回、「ワクチン接種と死亡との因果関係が否定できない」と認定されたケース 867 人と“薬害エイズ事件”により亡くなられた 568 人というデータを紹介した。
しかし、ワクチン関連死疑いはこれだけではない。
昨年 5 月、5 類以降により、厚生労働省が公表の仕方を変えたため総数が追いづらくなっている。
少し古くはなるが、厚労省によると、 4 月 21 日報告分では、新型コロナワクチンを接種したあとの医療機関からの「副反応疑い報告」は 37,091 件、その中で「重篤症例」は 9,014 件にのぼり、そのうち「死亡報告」は 2,204 件となっている。
国はコロナワクチンとの因果関係を α 、 β 、 γ で評価している。
α : ワクチンと死亡との因果関係が否定できないもの。原疾患との関係、薬理学的な観点や時間的な経過などの要素を勘案し、医学・薬学的観点から総合的に判断し、ワクチン接種が、事象(死亡)発現の原因となったことが否定できない症例。
【例】接種によると考えられるアナフィラキシーを発症した場合、アナフィラキシー自体は致死的な事象であり、状況により死亡に至る症例があれば α となりうる。
一方、ワクチン未接種者でも遇発的に起こり得る事象の場合、剖検所見等が得られて死因が判明しても、薬理学的観点や時間的な経過などの要素からは α とは判断し難い。
このような事象の因果関係評価は個別評価によらず、集団での評価に依らざるを得ない。
β : ワクチンと死亡との因果関係が認められないもの。 原疾患との関係、薬理学的な観点や時間的な経過などの要素を勘案し、医学・薬学的観点から総合的に判断し、ワクチン接種が、事象(死亡)発現の原因となったとは認められない症例。
γ : 情報不足等によりワクチンと死亡との因果関係が評価できないもの。 情報が十分でない、使用目的又は方法が適正でない等のためワクチン接種と事象(死亡)発現との因果関係の評価ができない症例。
【例】具体的な以下 2 つの場合
① 死因と考えられる事象の診断、事象とワクチンとの因果関係を判断するための情報が不足。
② 情報不足ではないが、得られた情報からは偶発的に起こったもの、合併症によるもの、併用薬によるものなどとの区別ができない。
このうち、 ① については、更なる情報収集が必要となるが、 ② については、情報を追加しても個別症例の因果関係評価には寄与しないため、個別評価によらず、集団での評価に依らざるを得ない。
結局、そのうち 99% を「因果関係不明」の γ だとしている。
そもそも副反応に関する国の調査はどう行われているのか?
そのプロセスは、一般には国民からはわかりにくく「ブラックボックス」ではないのか??
厚生労働省から公表されている副反応の報告・検証の仕組みを紹介する。
1. 副反応疑い報告の評価
医療機関報告及び企業報告(追加情報も含む)があるたび、専門家による因果関係の評価を行っている。
更に、報告のあった死因等に基づき、必要な場合は、 PMDA(※注 1 ) 若しくは厚生労働省から関連の医療機関や製造販売業者等に追加の調査を依頼し、それらの報告も同様に評価を行っている。
(※注 1 ) 医薬品医療機器総合機構。2004 年(平成 16 年)に設立された薬やワクチンの承認審査、副反応などの健康被害の「情報収集」などを担う機関。
2. 専門家の選定
PMDA において、呼吸器、循環器、神経、皮膚等の幅広い分野の臨床経験または、副作用若しくは副反応症例の因果関係評価の相応の経験を有する専門家(教授、准教授、講師クラス)を新型コロナワクチンの副反応評価を主に実施する人員として選定する。
3. 評価プロセス
2 名の専門家に評価を依頼し、評価が一致した場合はその結果を評価結果とする。
一致しない場合は、もう 1 名の専門家に評価を依頼し、 2 名の評価が一致したものを評価結果として採用する。
その後、外部専門家による評価が終わると、「厚生科学審議会(予防接種・ワクチン分科会/副反応検討部会)」にすべての情報が報告される。
メンバーは、医師や長年にわたり感染症研究に携わってきた専門家など 15 人で「報告内容は妥当かどうか」を検証する。
果たしてこれが機能しているのだろうか?
元々、医療の現場で様々な患者や病気と接する医師たちが、「コロナワクチンの影響じゃないか?」と疑い、考えたあげく国に報告したものなのである。
それが 99% が γ 判定とは・・・?
ただ、国はもうひとつ、接種との因果関係を調べる仕組みを設けている。
前回紹介した「予防接種健康被害救済制度」である。
接種後に副反応が疑われる症状が出た場合、本人や家族などが市町村に申請できる制度である。
認定を行うのは「疾病・障害認定審査会」と呼ばれる厚生労働省の専門家の審査会である。
ここで、医師や弁護士、感染症の専門家などがカルテの確認なども行い、因果関係をより詳しく調査することになっている。
一方、アメリカでは副反応の検証をどのように行っているのだろうか?
アメリカでは日本とは全く異なるアプローチを取っている。
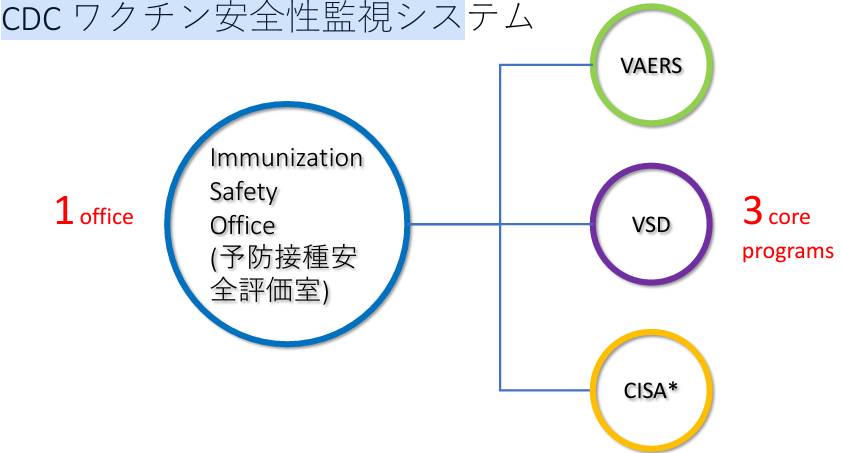
CDC 疾病対策センターの下に 3 つのプログラムが存在する。
Vaccine Adverse Event Reporting System ( VAERS )
• 早期に予防接種安全性に関する問題を発見するモニタリングシステム。
• 1990 年に創設、 CDC と FDA が管理。
• 予防接種後の有害事象の「自発的」報告を受けて解析する。
• 年間 40,000 ~ 50,000 件の報告。
• いかなる報告者でもレポート提出可能。
• 個人情報は保護される。
• オンラインでの報告が主。他の報告方法もあり。
• 一定の疾患には報告義務あり。
• 重症例については報告者に連絡してその後の経過について聴取し評価。
• 日本における PMDA の副反応疑い報告制度と同様のシステム。
Vaccine Safety Datalink ( VSD )
• 1990 年に創設。
• 9 つの民間の病院群とCDCの共同プロジェクト。
• 1,200 万人の人口をカバーする。(アメリカ全体の 3.7% )
• 仮説検証のための疫学研究が可能。( Population-based study )
• 30 年以上の実績をもつ強固な官民のコラボレーション。
• 極めて高い正確性を保った予防接種データ。
• 電子カルテにアクセスしてさらなる検証が可能。
• 厳重な個人情報保護の管理。
• 各データ地区に MD (※注 1 )、 PhD (※注 2 )、 MPH (※注 3 )、 データ専門家等の専門グループ。
• 多岐にわたる研究デザインを施行可能。
(※注 1 ) Medical Docto の略称。医師。
(※注 2 ) Doctor of Philosophy の略称。博士。
(※注 3 ) Master of Public Health の略称。公衆衛生大学院修。
Clinical Immunization Safety Assessment ( CISA )
• 2001 年に設立.
• 個々の患者レベルでの有害事象(ワクチンが原因かどうかは明らかでない場合でも、ワクチン接種後に懸念される副作用や健康上の問題)を追求。
• 個々の患者に関する複雑なワクチンの安全性に関する質問がある米国の医療提供者へのコンサルティングを提供。
• ワクチンの安全性に関する重要な問題を調査するために、ワクチンの安全性に関する臨床研究を実施。
• 米国の医療提供者および保健局を支援。
• 新たなワクチンの安全性に関する問題の評価において CDC とそのパートナーを支援。
• ワクチンの安全性をより深く追求し、予防接種後の有害事象の予防戦略(ワクチン接種後のめまいやめまいを防ぐ方法など)を見つけるために、臨床研究調査を実施。
上記、 3 つのプログラムを中心に情報を集め、 Immunization safety Office (予防安全評価室)に集約され、利点と欠点を検証しながら、ワクチンの安全性をより確実なものにしていくというシステムが構築されている。
ワクチン後進国の日本から比べると、何世代先に進んでいるのだろうかと思ってしまう。
次回へ・・・。













