前回の続き・・・。
■ 研究内容
細胞不死化酵素として知られる‟テロメラーゼ”は、‟テロメア”の長さを維持することで細胞に不死化能を付与することが知られてきました。
しかし、最近では、‟テロメラーゼ”にはこの細胞不死化酵素としての役割以外にも異なる酵素活性(=‟テロメラーゼ”の新たな機能)が存在することが示唆されてきましたが、その詳細は分かっていませんでした。
本共同研究グループは、‟テロメラーゼ”との関連が示されている肝臓がんと膵臓がん患者からの手術検体等を用いた解析を行いました。
その結果、‟テロメラーゼ”の新たな‟がん”化機能が肝臓がんや膵臓がんのうちでも悪性度が高いものほど活発であり、この機能の作用が強いほど予後が悪いことを明らかにしました(図 2 ,図 3 )。
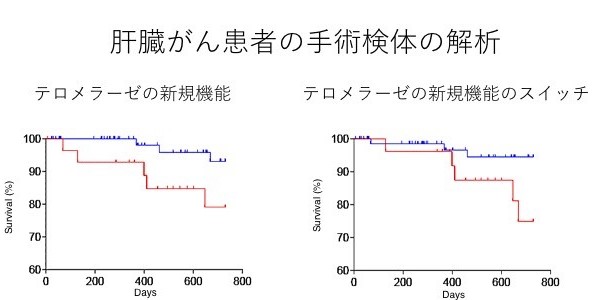
図 2 :肝臓がん患者 100 例の手術検体を用いた解析
左:‟テロメラーゼ”の新たな機能の作用が強い患者群(赤色)とその作用が弱い患者群(青色)では、新たな機能の作用が強い患者群(赤色)の方が統計学的に有意に予後が悪かった。
右:‟テロメラーゼ”の新規機能のスイッチを入れる分子である CDK1 の作用が強い患者群(赤色)とその作用が弱い患者群(青色)では、CDK1 の作用が強い患者群(赤色)の方が統計学的に有意に予後が悪かった。
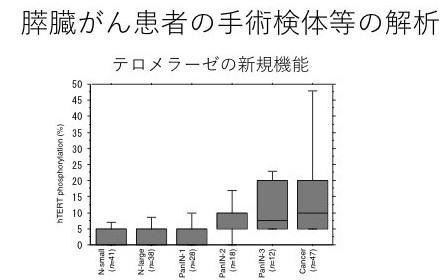
図 3 :膵臓がん患者約 50 例の手術検体等を用いた解析
膵臓がんでは正常(左側)から前がん病変、‟がん”(右側)へと病気が進むにつれて、‟テロメラーゼ”の新たな機能が活発に作用していることが確認された。
この‟テロメラーゼ”の新たな機能のスイッチがどのように制御されるのかについて調べたところ、 CDK1(※注 3 )という分子がテロメラーゼをリン酸化(※注 4 )することでスイッチを入れていることを見いだしました。
(※注 3 ) Cyclin Dependent Kinase-1(サイクリン依存性キナーゼ− 1 )の略。細胞は DNA 複製と DNA 分配とを繰り返して細胞分裂することが知られている。複製と分裂の繰り返しの単位のことを細胞周期と呼び、大きく分けて 4 つの時期に分けることができる。細胞周期のそれぞれの時期に、規則正しく正確にタンパク質の機能を発揮(スイッチオン)させたり機能を抑制(スイッチオフ)させることで、正確な細胞分裂が保証されている。 CDK1 は細胞周期の分裂期にのみ作用を発揮するキナーゼであり、キナーゼは作用する標的のタンパク質のリン酸化を司っている。
(※注 4 ) タンパク質はその機能を発揮したり機能を停止したりするために、リン酸化という化学修飾を受ける。タンパク質にリン酸基を付ける化学修飾のことをリン酸化、逆にリン酸基を外す化学修飾のことを脱リン酸化という。リン酸基をタンパク質に付加する化学修飾を行う酵素を総称してキナーゼという。
そこで、‟テロメラーゼ”の新たな機能のスイッチを入れる分子である CDK1 の機能を阻害してみると、細胞不死化酵素としての機能には何の影響も及ぼさない一方、‟テロメラーゼ”の新たな機能は完全に阻害されることを確認しました(図 4 )。
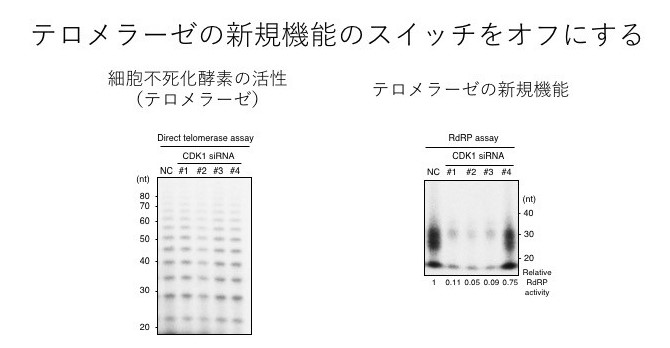
図 4 :‟テロメラーゼ”が持つ機能の検証
‟テロメラーゼ”がの新たな機能のスイッチを入れる分子である CDK1 の機能を抑えて、細胞不死化酵素と新たな機能のそれぞれの作用の強さを検証した。
いずれのパネルも #1 , #2 , #3 のレーンが効率的に CDK1 の機能が押さえ込まれている細胞を示す。
左:CDK1の機能を抑えても、細胞不死化酵素の作用には影響がない。
右:CDK1の機能を抑えると、テロメラーゼの新たな機能の作用が極端に弱まる。 という結論が導き出されました。
これらのことから、このスイッチは、‟テロメラーゼ”の新たな機能のオン、オフをコントロールしていることが確認できました。
これまでは、‟テロメラーゼ”は、細胞不死化酵素としてがん細胞のがん細胞たる特徴を制御していると考えられていましたが、今回の発見から、‟テロメラーゼ”の新たな機能が細胞の‟がん”化に何らかの影響を及ぼしているという疑問が出てきたため、その疑問に対する答えを探すために研究を続けました。
最近では、遺伝子編集技術を用いることで、細胞内の任意の遺伝子を改変できることから、この技術を用いて、‟テロメラーゼ”の新たな機能のみが働かなくなった細胞を作製しました。
その結果、この細胞では、正常な細胞と同じようにマウスで腫瘍を作らなくなりました(図 50 )。
これらの結果を総合的に判断すると、「‟テロメラーゼ”の新たな機能」だけを働かなくする(=スイッチをオフにする)だけで、もはや‟がん”細胞としての特徴を持たなくなってしまう。
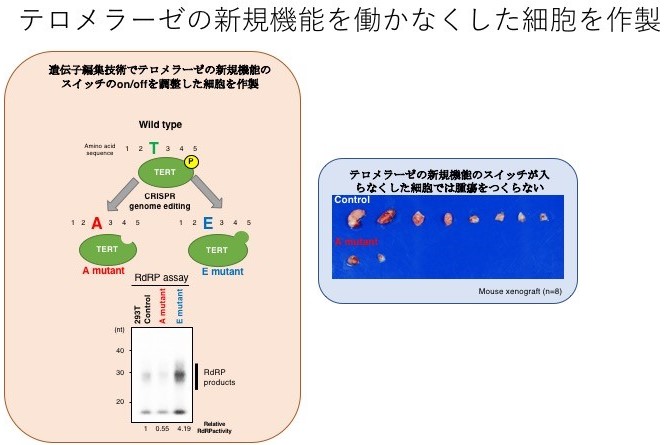
図 5 :遺伝子編集技術を用いた、‟テロメラーゼ”の新たな機能のスイッチが入らなくなった細胞の作製
左:赤色で示した部分( A )が遺伝子編集技術で改変した部分であり、この細胞ではどれほど CDK1 が作用を発揮しようとしても、‟テロメラーゼ”の新たな機能のスイッチは入らなくなっている。
右:この細胞( A 細胞)をマウスに移植してももはや腫瘍を作ることはなくなった。
■ 展望
近年の世界的規模による、‟がん”遺伝子情報の大規模な解析によって、多くの‟がん”種で‟テロメラーゼ”分子の‟がん”治療に対する標的としての重要性が再認識されてきた一方で、過去 20 年以上にわたって行われてきた細胞不死化酵素としての‟テロメラーゼ”を標的とした治療薬の開発は、残念ながら不成功に終わっています。
このような中で、本研究により、‟テロメラーゼ”の新たな機能が、これまで想定していなかった分子群の関与により制御され、細胞の‟がん”化に深く関与していることを発見したことは、肝炎関連肝臓がんや膵臓がんでの全く新しい‟がん”治療法の開発につながると期待されます。
さらには、‟テロメラーゼ”の新たな機能は広く‟がん”種横断的に関わる可能性が考えられることから、肝臓がんや膵臓がんのみならず、多くの‟がん”種に効果を発揮する新たな薬剤の開発につながる可能性も期待されます。
がんとの闘病のいて新たなステージが始まることを期待しつつ次回へ続く。













